Opakowania farmaceutyczne
Opakowania farmaceutyczne odgrywają nieocenioną rolę w całym cyklu życia produktu leczniczego, od momentu jego produkcji, przez transport i dystrybucję, aż po przechowywanie w aptece i stosowanie przez pacjenta. Ich podstawowym zadaniem jest ochrona substancji czynnej przed szkodliwym działaniem czynników zewnętrznych, takich jak światło, wilgoć, tlen czy zanieczyszczenia mikrobiologiczne. Bez odpowiedniego zabezpieczenia, leki mogłyby szybko stracić swoje właściwości terapeutyczne, a co gorsza, stać się niebezpieczne dla zdrowia. Jakość opakowania bezpośrednio przekłada się na stabilność farmaceutyczną preparatu, gwarantując jego skuteczność i bezpieczeństwo przez cały okres ważności.
Wybór odpowiedniego materiału i konstrukcji opakowania farmaceutycznego jest procesem złożonym, uwzględniającym specyfikę danego leku. Różne formy farmaceutyczne – tabletki, kapsułki, proszki, płyny, maści czy preparaty do wstrzykiwań – wymagają odmiennych rozwiązań ochronnych. Kluczowe jest zapewnienie szczelności, która zapobiega migracji substancji i chroni przed dostępem powietrza i wilgoci. Ponadto, opakowania muszą być odporne na uszkodzenia mechaniczne, aby zapobiec stłuczeniu ampułek czy zgnieceniu blistrów podczas transportu. Należy również pamiętać o aspektach związanych z łatwością otwierania i zamykania, zwłaszcza w przypadku opakowań dla osób starszych lub mających problemy z manualnymi zdolnościami.
Regulacje prawne dotyczące opakowań farmaceutycznych są niezwykle restrykcyjne i stale ewoluują, aby zapewnić najwyższy poziom bezpieczeństwa dla pacjentów. Normy dotyczące materiałów używanych do produkcji opakowań, procesów sterylizacji, a także wymagań druku i znakowania, są ściśle określone przez międzynarodowe i krajowe organy nadzorcze. Producenci leków muszą spełniać te wytyczne, aby ich produkty mogły być dopuszczone do obrotu. Obejmuje to również zapewnienie integralności opakowania wtórnego, które chroni opakowanie pierwotne i zawiera kluczowe informacje dla użytkownika, takie jak dawkowanie, przeciwwskazania czy numer serii.
Wymagania stawiane nowoczesnym opakowaniom farmaceutycznym
Współczesne opakowania farmaceutyczne muszą sprostać rosnącym wymaganiom dotyczącym nie tylko ochrony produktu, ale także jego identyfikacji i zapewnienia bezpieczeństwa użytkownika. Jednym z kluczowych aspektów jest zabezpieczenie przed fałszerstwami. W obliczu rosnącej skali podrabiania leków, opakowania stają się pierwszą linią obrony. Technologie takie jak hologramy, unikalne kody kreskowe, znaczniki RFID czy specjalne farby zabezpieczające, utrudniają nielegalne kopiowanie i pozwalają na szybką weryfikację autentyczności produktu. Te rozwiązania nie tylko chronią pacjentów przed przyjmowaniem nieskutecznych lub szkodliwych substancji, ale także chronią reputację producentów i integralność rynku farmaceutycznego.
Kolejnym istotnym elementem jest zapewnienie pełnej informacji o produkcie. Opakowania wtórne, czyli te zewnętrzne, zazwyczaj w formie kartoników, muszą zawierać wszystkie niezbędne dane w sposób czytelny i zrozumiały dla pacjenta. Dotyczy to nazwy leku, substancji czynnej, dawki, sposobu podania, przeciwwskazań, działań niepożądanych, warunków przechowywania, daty ważności oraz numeru serii. W ostatnich latach coraz większą wagę przykłada się do czytelności druku, stosując większe czcionki i kontrastowe kolory, co jest szczególnie ważne dla osób z wadami wzroku. Dodatkowo, coraz częściej stosuje się kody QR, które po zeskanowaniu smartfonem przekierowują do szczegółowych informacji o leku, ulotki w wersji elektronicznej czy nawet filmów instruktażowych dotyczących sposobu użycia.
Nie można zapominać o aspekcie ekologicznym. Producenci opakowań farmaceutycznych coraz częściej poszukują materiałów biodegradowalnych, nadających się do recyklingu lub pochodzących z odnawialnych źródeł. Jednocześnie, muszą one spełniać rygorystyczne normy dotyczące kontaktu z żywnością i lekami, co oznacza, że wybór materiałów jest ograniczony. Wiele opakowań farmaceutycznych jest nadal wykonanych z tworzyw sztucznych, ale firmy coraz chętniej inwestują w badania nad innowacyjnymi, bardziej przyjaznymi dla środowiska alternatywami, które nie kompromitują bezpieczeństwa i stabilności produktu. Wdrożenie takich rozwiązań wymaga jednak czasu i znaczących inwestycji.
Innowacyjne rozwiązania w opakowaniach dla przemysłu farmaceutycznego

Kolejnym trendem jest personalizacja opakowań. Dzięki zaawansowanym technologiom druku cyfrowego, możliwe staje się produkowanie opakowań z indywidualnymi informacjami dla pacjenta, takimi jak jego imię, zalecana dawka czy harmonogram przyjmowania leków. Jest to szczególnie ważne w przypadku terapii skojarzonych lub leków o wąskim indeksie terapeutycznym, gdzie precyzja dawkowania ma kluczowe znaczenie. Personalizacja może również obejmować dostosowanie języka i formy przekazu informacji do konkretnej grupy odbiorców, zwiększając tym samym zrozumiałość i dostępność leczenia. Ten kierunek rozwoju pozwala na budowanie silniejszej relacji między pacjentem a produktem leczniczym.
Materiały opakowaniowe również podlegają ciągłym innowacjom. Obok tradycyjnych tworzyw sztucznych i szkła, coraz częściej wykorzystywane są zaawansowane kompozyty i nanomateriały, które oferują lepsze właściwości barierowe, zwiększoną wytrzymałość mechaniczną i mniejszą wagę. Badane są również rozwiązania oparte na materiałach odnawialnych, takich jak biopolimery pochodzenia roślinnego, które mogą stanowić ekologiczną alternatywę dla tradycyjnych opakowań. Rozwój technologii druku 3D otwiera nowe możliwości w projektowaniu opakowań o skomplikowanych kształtach i funkcjonalnościach, dostosowanych do specyficznych potrzeb terapeutycznych. Te postępy technologiczne pozwalają na tworzenie opakowań, które są nie tylko bezpieczne i funkcjonalne, ale także bardziej zrównoważone i przyjazne dla użytkownika.
Znaczenie certyfikacji i zgodności w branży opakowań farmaceutycznych
W branży opakowań farmaceutycznych certyfikacja i ścisłe przestrzeganie obowiązujących norm i regulacji prawnych stanowią fundament bezpieczeństwa i jakości produktów leczniczych. Proces uzyskiwania certyfikatów, takich jak ISO 9001 czy specyficzne dla branży farmaceutycznej GMP (Good Manufacturing Practice), jest niezbędny dla producentów opakowań, którzy chcą dostarczać swoje wyroby firmom farmaceutycznym. Certyfikaty te potwierdzają, że proces produkcji jest kontrolowany na każdym etapie, od doboru surowców, poprzez sam proces wytwarzania, aż po pakowanie i dystrybucję. Zapewniają one, że opakowania są produkowane w warunkach higienicznych, spełniają określone standardy jakościowe i są wolne od zanieczyszczeń, które mogłyby negatywnie wpłynąć na stabilność i bezpieczeństwo leku.
Zgodność z przepisami prawa farmaceutycznego, w tym z wytycznymi europejskimi (np. EMA) i amerykańskimi (np. FDA), jest kluczowa dla każdego podmiotu działającego w tym sektorze. Dotyczy to nie tylko samych opakowań pierwotnych, które mają bezpośredni kontakt z produktem leczniczym, ale także opakowań wtórnych i materiałów informacyjnych. Należy zapewnić, że wszystkie nadruki i informacje zawarte na opakowaniu są zgodne z zatwierdzoną charakterystyką produktu leczniczego i ulotką dla pacjenta. W przypadku opakowań przeznaczonych na rynek europejski, kluczowe jest również przestrzeganie wymagań dotyczących zabezpieczeń przed fałszerstwami, wprowadzonych w ramach dyrektywy FMD (Falsified Medicines Directive), która nakłada obowiązek stosowania unikalnych identyfikatorów i zabezpieczeń uniemożliwiających ponowne użycie opakowania.
Kontrola jakości jest procesem ciągłym, obejmującym szereg testów i analiz mających na celu weryfikację właściwości fizycznych, chemicznych i biologicznych opakowań. Obejmuje to testy szczelności, odporności na penetrację wilgoci i tlenu, stabilności materiału w określonych warunkach temperaturowych i wilgotnościowych, a także badania migracji substancji ze ścianek opakowania do produktu leczniczego. Dodatkowo, przeprowadzane są testy potwierdzające zgodność materiałów z normami dotyczącymi kontaktu z żywnością i lekami (np. rozporządzenia UE dotyczące materiałów i przedmiotów przeznaczonych do kontaktu z żywnością). Rzetelne zarządzanie jakością i utrzymywanie wysokich standardów produkcyjnych jest nie tylko wymogiem prawnym, ale także kluczowym czynnikiem budującym zaufanie wśród partnerów biznesowych i konsumentów.
Opakowania farmaceutyczne a bezpieczeństwo pacjentów i środowiska
Bezpieczeństwo pacjentów jest nadrzędnym celem wszystkich działań podejmowanych w zakresie projektowania, produkcji i stosowania opakowań farmaceutycznych. Odpowiednie opakowanie chroni lek przed degradacją, która mogłaby prowadzić do utraty jego mocy terapeutycznej lub co gorsza, do powstania toksycznych produktów rozkładu. Szczelność opakowań, zwłaszcza tych zawierających leki w postaci płynnej lub proszku, zapobiega zanieczyszczeniu mikrobiologicznemu, które może być niebezpieczne dla zdrowia, szczególnie w przypadku preparatów do stosowania parenteralnego. W przypadku leków stosowanych doustnie, opakowania takie jak blistry czy butelki z zabezpieczeniem przed otwarciem przez dzieci (child-resistant closures) odgrywają kluczową rolę w zapobieganiu przypadkowemu spożyciu przez najmłodszych.
Aspekt środowiskowy opakowań farmaceutycznych zyskuje na znaczeniu. Producenci coraz częściej zwracają uwagę na potencjalny wpływ materiałów opakowaniowych na środowisko naturalne, zarówno na etapie ich produkcji, jak i po utylizacji. W związku z tym, obserwuje się wzrost zainteresowania materiałami pochodzącymi z recyklingu, biodegradowalnymi lub wykonanymi z surowców odnawialnych. Wyzwaniem pozostaje jednak znalezienie takich materiałów, które jednocześnie spełniałyby rygorystyczne wymagania dotyczące ochrony leków i bezpieczeństwa kontaktu z produktami farmaceutycznymi. Rozwój technologii pozwala na tworzenie opakowań, które są lżejsze, co zmniejsza ślad węglowy podczas transportu, a także łatwiejsze do segregacji i przetworzenia po zużyciu.
Proces utylizacji opakowań farmaceutycznych wymaga szczególnej uwagi. Zużyte opakowania po lekach, zwłaszcza te zawierające pozostałości substancji czynnych, nie powinny trafiać do zwykłych odpadów komunalnych ani do kanalizacji, ponieważ mogą zanieczyszczać glebę i wodę. Wiele krajów wprowadza systemy zbiórki leków przeterminowanych i ich opakowań, które są następnie bezpiecznie unieszkodliwiane. Edukacja pacjentów na temat prawidłowej utylizacji jest kluczowa dla minimalizacji negatywnego wpływu opakowań farmaceutycznych na środowisko. Świadomość ekologiczna konsumentów i nacisk na zrównoważone rozwiązania napędzają innowacje w tej dziedzinie, prowadząc do tworzenia bardziej odpowiedzialnych ekologicznie opakowań.
Wpływ opakowań farmaceutycznych na stabilność i okres ważności leków
Stabilność farmaceutyczna jest jednym z kluczowych czynników decydujących o skuteczności i bezpieczeństwie produktu leczniczego, a opakowanie odgrywa w jej utrzymaniu fundamentalną rolę. Substancje czynne zawarte w lekach mogą być wrażliwe na różne czynniki zewnętrzne, takie jak tlen obecny w powietrzu, wilgoć, promieniowanie UV lub zmiany temperatury. Niewłaściwe opakowanie, które nie zapewnia odpowiedniej bariery ochronnej, może prowadzić do przyspieszonej degradacji substancji aktywnej, co skutkuje obniżeniem jej stężenia, a tym samym zmniejszeniem skuteczności terapeutycznej leku. W skrajnych przypadkach, procesy degradacji mogą prowadzić do powstania produktów ubocznych o potencjalnie szkodliwym działaniu dla organizmu pacjenta.
Okres ważności leku, czyli czas, przez który produkt zachowuje swoje właściwości terapeutyczne i jest bezpieczny do stosowania, jest ściśle powiązany z jego stabilnością. Producenci przeprowadzają szczegółowe badania stabilności, które pozwalają określić, jak długo lek pozostaje w granicach specyfikacji jakościowej w określonych warunkach przechowywania. Opakowanie jest integralną częścią tych badań, ponieważ to ono ma za zadanie chronić lek przed czynnikami przyspieszającymi jego rozkład. Wybór odpowiedniego materiału opakowaniowego, takiego jak szkło farmaceutyczne, specjalne tworzywa sztuczne o wysokich właściwościach barierowych, czy też zastosowanie dodatkowych zabezpieczeń, jak na przykład absorbenty wilgoci czy folie aluminiowe, jest kluczowe dla osiągnięcia wymaganego okresu ważności produktu. Każdy lek wymaga indywidualnego podejścia, uwzględniającego jego specyficzną wrażliwość.
Dla zapewnienia stabilności i maksymalnego okresu ważności, stosuje się różnorodne technologie opakowaniowe. Przykładowo, dla leków wrażliwych na światło, stosuje się nieprzezroczyste materiały opakowaniowe, takie jak ciemne szkło lub folie metalizowane. Leki wrażliwe na wilgoć mogą być pakowane w blistry z folii aluminiowej lub butelki z uszczelkami zapewniającymi hermetyczność. W przypadku preparatów sterylnych, kluczowe jest zapewnienie jałowości opakowania oraz jego integralności przez cały okres przechowywania. Procesy takie jak liofilizacja (suszenie przez wymrażanie), stosowane w celu zwiększenia stabilności niektórych leków, również wymagają specjalistycznych opakowań, które chronią produkt przed wilgocią oraz ułatwiają jego późniejsze przywrócenie do formy użytkowej. Inwestycja w wysokiej jakości opakowania jest więc bezpośrednią inwestycją w jakość i bezpieczeństwo leku.
Rodzaje opakowań pierwotnych i wtórnych dla produktów farmaceutycznych
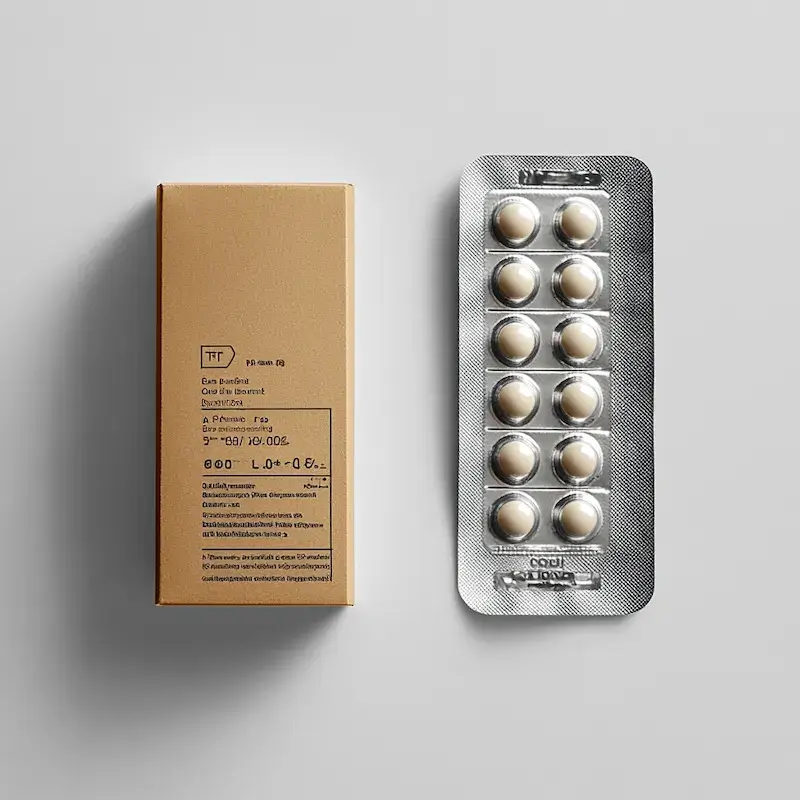
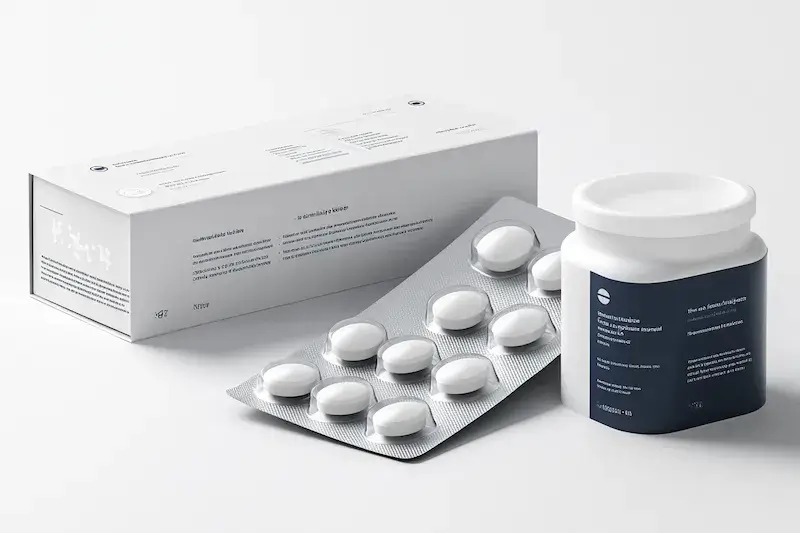
Opakowania farmaceutyczne dzielą się na dwie główne kategorie: opakowania pierwotne i opakowania wtórne, z których każde pełni specyficzne funkcje. Opakowanie pierwotne to to, które ma bezpośredni kontakt z produktem leczniczym. Jego głównym zadaniem jest ochrona substancji czynnej przed czynnikami zewnętrznymi, takimi jak tlen, wilgoć, światło czy zanieczyszczenia mikrobiologiczne, a także zapewnienie jego stabilności i bezpieczeństwa przez określony czas. Do najczęściej stosowanych opakowań pierwotnych należą: szklane fiolki i ampułki, które są idealne dla płynnych preparatów do wstrzykiwań, tabletek i kapsułek, ze względu na ich obojętność chemiczną i niski współczynnik przepuszczalności. Blistry, wykonane zazwyczaj z PVC, PET lub aluminium, są powszechnie stosowane do pakowania tabletek i kapsułek, zapewniając indywidualne zabezpieczenie każdej dawki. Tuby, najczęściej aluminiowe lub plastikowe, służą do pakowania maści, kremów i żeli. Butelki, wykonane ze szkła lub tworzyw sztucznych, są używane do przechowywania płynów doustnych, zawiesin czy kropli.
Opakowanie wtórne, znane również jako opakowanie zbiorcze lub zewnętrzne, pełni funkcję ochronną dla opakowania pierwotnego oraz stanowi nośnik kluczowych informacji dla pacjenta i personelu medycznego. Zazwyczaj jest to kartonik, który zawiera jedną lub więcej jednostek opakowania pierwotnego. Na opakowaniu wtórnym umieszcza się nazwę leku, jego dawkę, substancję czynną, numer serii, datę ważności, a także szczegółowe informacje dotyczące dawkowania, przeciwwskazań, działań niepożądanych i sposobu przechowywania. Opakowanie wtórne odgrywa również ważną rolę w zabezpieczeniu przed fałszerstwami, często wykorzystując specjalne nadruki, hologramy lub inne elementy utrudniające nielegalne kopiowanie. Dodatkowo, opakowanie wtórne ułatwia transport i przechowywanie leków w aptekach i hurtowniach, zapewniając ich ochronę przed uszkodzeniami mechanicznymi i innymi czynnikami zewnętrznymi podczas dystrybucji.
Oprócz opakowań pierwotnych i wtórnych, istnieją również opakowania trzeciorzędowe, służące do transportu i magazynowania dużych ilości produktów farmaceutycznych. Są to zazwyczaj kartony zbiorcze, palety owinięte folią stretch lub kontenery transportowe. Ich głównym zadaniem jest zapewnienie bezpieczeństwa ładunku podczas transportu i ułatwienie manipulacji w magazynach. Wybór odpowiedniego rodzaju i materiału opakowania jest kluczowy dla zachowania jakości, bezpieczeństwa i skuteczności produktu leczniczego przez cały okres jego przydatności do użycia. Każdy element opakowania, od materiału po projekt graficzny, musi spełniać rygorystyczne normy i przepisy prawa farmaceutycznego.
Wpływ OCP przewoźnika na bezpieczeństwo łańcucha dostaw leków
OCP, czyli Operatora Centrum Przetwarzania, w kontekście farmaceutycznym, odgrywa kluczową rolę w zapewnieniu bezpieczeństwa i integralności łańcucha dostaw leków. Jest to podmiot odpowiedzialny za zarządzanie i obsługę magazynów wysokiego składowania, w których przechowywane są produkty lecznicze przed ich dystrybucją do aptek, szpitali czy innych punktów odbioru. Odpowiednie zabezpieczenie tych centrów, w tym kontrola dostępu, monitoring wizyjny oraz stosowanie odpowiednich warunków temperaturowych i wilgotnościowych, jest absolutnie kluczowe dla ochrony leków przed kradzieżą, uszkodzeniem lub zepsuciem. OCP musi również zapewnić ścisłą identyfikowalność każdej partii leku, od momentu przyjęcia do magazynu, aż po jego wydanie, co jest niezbędne do szybkiego reagowania w przypadku ewentualnych problemów jakościowych lub wycofań produktów z rynku.
Bezpieczeństwo fizyczne magazynów, którymi zarządza OCP, jest priorytetem. Obejmuje to zarówno zabezpieczenie przed nieuprawnionym dostępem osób trzecich, jak i ochronę przed czynnikami zewnętrznymi, takimi jak pożar, powódź czy inne zdarzenia losowe. Nowoczesne centra przetwarzania wyposażone są w zaawansowane systemy alarmowe, kontrolę dostępu opartą na kartach lub biometrii, a także systemy gaśnicze. Równie ważne jest utrzymanie odpowiedniego klimatu w magazynach, szczególnie w przypadku leków wymagających przechowywania w obniżonej temperaturze (tzw. łańcuch chłodniczy). OCP jest odpowiedzialne za monitorowanie i utrzymanie tych warunków, często z wykorzystaniem specjalistycznych chłodni i systemów klimatyzacji, które są regularnie kalibrowane i serwisowane. Każde odstępstwo od normy musi być natychmiast rejestrowane i analizowane.
W kontekście OCP, istotne jest również przestrzeganie zasad Dobrej Praktyki Dystrybucyjnej (GDP – Good Distribution Practice). Oznacza to, że wszystkie procesy związane z magazynowaniem, kompletacją zamówień i wysyłką leków muszą być zgodne z najwyższymi standardami jakościowymi i bezpieczeństwa. OCP musi posiadać odpowiednio przeszkolony personel, który zna procedury postępowania w sytuacjach awaryjnych i potrafi obsługiwać skomplikowane systemy magazynowe. Dokumentacja wszystkich procesów, od przyjęcia towaru po jego wydanie, musi być prowadzona skrupulatnie, co pozwala na pełną identyfikowalność i kontrolę nad całym łańcuchem dostaw. Współpraca OCP z producentami leków i dystrybutorami jest kluczowa dla zapewnienia, że leki docierają do pacjentów w nienaruszonej formie i zachowują swoje właściwości terapeutyczne.
„`